�ߝ�ȷ�ɢ�{Ⱦ�ϏUˮ�ĝ�ʽ�����о�
ժҪ:��2L�߉��gЪ��������,�о��˝�ʽ�������ߝ�ȷ�ɢ�{Ⱦ�ϏUˮ̎����Ч���������ضȵ�Ӱ푺̈́����W�������о�����:�ض��Ƿ�ɢ�{Ⱦ�ϏUˮ��ʽ�������P�IӰ�����,��������������Ч�������;�MˮCODCr46710mg/L��255�桢1.25����Փ�������·���2h,CODCrȥ�����_72.1%,���������@�����,ɫ����ȫ��ȥ����������������ͨ�Ä����Wģ��,��������˝�ʽ�����^�̡�
����
�P�I�~:��ɢ�{Ⱦ�ϏUˮ����ʽ������CODCr�������Wģ��
����
Ⱦ�ϷN�������ɢ�����ԡ��A�ԡ����ԡ�ֱ�ӡ�߀ԭ�����Ժ���x�ӵ�ʮ���,Ʒ�N�_500��N��Ⱦ�ϏUˮһ�㺬�б�ϵ����ϵ������ϵ���u�������������ͷ���ЙC��,�ЙC���Ⱥ�ɫ�ȸߡ��y�������|�ࡣһ����ö����������ﻯ��̎����ˇ,�����y�����ЙC��̎��Ч���^����ĵ�Ⱦ�ϏUˮȡ�Խ��Kij�����S,ԓ�S���a��ɢ�m60#Ⱦ��,�������ͷ�ɢȾ��,�������������c���������������������Ҵ��܄��пs�϶���,�����܄����ŷŵďUˮ�к��д�������ϵ���Ҵ���ԭ�Ϻ����g�w,�ЙC���ȸ�,�������Բ�,���ڵ��ߝ���y�����ЙC�Uˮ,Ŀǰȱ��������Ч��̎�����g��
����
��ʽ����(WetAirOxidation,WAO)�����^�ߜض�(125��350��)�͉���(0.5��20MPa)��,�Կ՚������������,��Һ�����ЙC�������ֽ�ɟo�C���С�����ЙC��ķ������c��Ҏ�������,��ʽ���������m���ЙC���ȸߡ�̎��Ч�ʸߡ�������Ⱦ�͡������ٶȿ졢�ɻ������������|�����c[1],����ܵ��h����ďV����ҕ����һ��WAO������Strehlenert��1911�����,20���o60����Ժ�,WAO�ڻ��ռ��{���WƷ����ˮ�S���������ͻ���̿�����ȵõ��ˑ���[2],��20���o70�������,WAO���о��͑��÷���Ѹ�ٔUչ���ж��к��Uˮ���U���̎��,������̎�����ӡ��衢����ж��к����|�����д������īI��,�о����ݏ��m�������뵽�����C���������W[3��5]��
����
�����о��˷�ɢ�{Ⱦ�ϏUˮ��ʽ������̎��Ч���̈́����W����,�鹤�̑����ṩ��Փ�����ͼ��gָ����
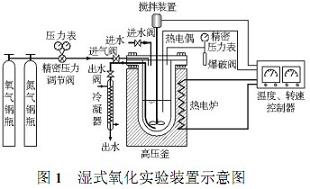 |
1����b�á������c���ˮ�|
1.1������b��
����
����b����D1��ʾ����������FYX22a���������D����߉���(2L),�������������b�á��ӟ�t����sϵ�y�Ϳ���ϵ�y�ȽM�ɡ�
����
��������ֱ���{��늙C���Ӵ���������M�Д���,���ɿ������{���D�١������ض��ɼӟ�tͨ�^���ܿ���������(±2��)��
1.2������
����
�����gЪ��ʽ����,�����������⡣ԇ�r���ȼ���400mLˮ��,�ܷⷴ����,���붨�������ӟ�,�_���A�O�ضȕr�_�����貢�S����500r/min,���A���r�̏�������ȡ�ӷ�����
1.3��ˮ�|��������
����
CODCr�������t��⛷�;TOC����TOC�����x�y��;pH���þ��ܔ��@���Ӌ�y����
1.4���Uˮˮ�|
����
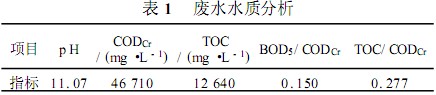
��ɢ�{Ⱦ�ϏUˮˮ�|ָ��Ҋ��1��
 |
2�����Y���cӑՓ
 |
2.1���ضȌ���ʽ������Ӱ�
����
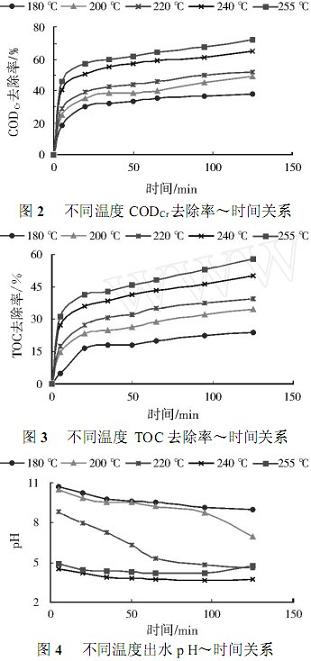
�ڹ���PO2=1.25PO23(��Փ����)�¿����˜ضȌ�WAO��Ӱ�(�D2��4)��
����
�Y������:�ٜضȌ��ЙC��������Ӱ푷dz��@��,CODCr��TOCȥ�����S�ض��������@���;��ǰ20min�����ٶȿ�,�����ɻ���������,�˺��ٶ��в�ͬ�̶Ȝp��;��CODCrȥ���ʾ�����TOCȥ����,TOC�����М���
����
�D4�@ʾ��WAO���g�a���ЙC���cԭˮ�ЉA�����|�����LҎ��:�͜���,�ЙC��������CO2�ٶȺ��������ЙC����ٶ��Լ��ЙC��������CO2���ٶȾ��^��,���a���ٶȿ����������ٶ�,�ЙC��e�ۺ͉A���ЙC�������ʹpH�½�;�ض�����,�ЙC�������ٶȼӿ�,�����220����,pH�½��^��;240���255��r����������A���|���ӽ����Lƽ��,�������ڿ��ЙC���Ƚ���,�a���ٶ��½�,��K��ˮ��pH����������
2.2����ʽ������ˮˮ�|�c��������׃��
����
�Uˮ��ʽ������ˮˮ�|���2��ʾ���Y������:��ʽ������,B/C���@�����,�Ҝض�Խ��,��߷���Խ��,���B/C�_0.691,�������Եõ��@������,�@�����Uˮ�д���ӻ��y�����ЙC����������CO2��С�����������ЙC��;����,��ˮ�ʟoɫ��,ÓɫЧ���dz��@��(ɫ�ȏ�5�f������50������)������������ߺ�ɫ�ȵ�ȥ��������m����̎���ṩ�˘O�������ėl����
2.3����ʽ���������W����
����
�����W�о������ڽ�ʾ�����v��,�˽ⷴ���C�������ٲ��E,�鹤���OӋ�ṩָ�����A�y�����Y����ͨ�Ä����Wģ��[6](�D5��ʽ1)�����������W�����P�˺��^�ЙC�����������g�a���ЙC��׃��,�^�õؽ�ʾ��һ���ЙC���ʽ����Ҏ�ɡ�
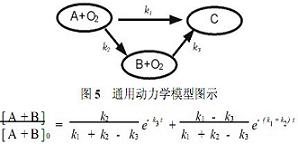 |
ʽ��,A���ʼ�ЙC��Ͳ����������g�a��(��CODCr��TOC��ʾ),B��ͼ��ЙC��(��CODCr��TOC��ʾ),C��������K�a��,��CO2,ʽ����0��ʾ��ʼֵ,�Ҽٶ�[B]0=0��
����
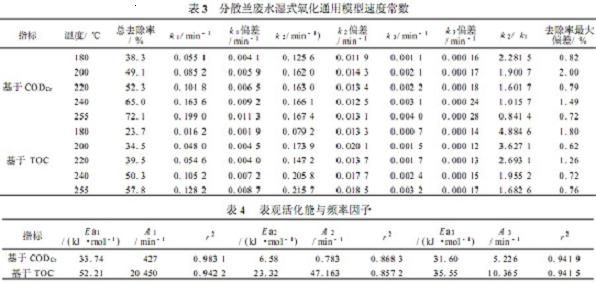
���ڈD2��3���Y��,����ͨ�Ä����Wģ�͔M�ό���,��Levenberg2Marquardt(Microcalorigin����)�Ǿ������Ӌ��k1��k2��k3�����3��
����
��3����:��k1��k3�S�ض������@������,k2�S�ض�׃���^С,���������������ЙC��ֱ�������ɽK�a������g�a��������CO2;�����cֵk2/k1��������;�����x����,ԓֵԽ��,��������ƫ�����������g�a�﷽��,��֮�tƫ����ֱ������CO2����,k2/k1�S�ض��������@�pС,��Ҋ�͜��·���ƫ�����������g�a��ͼ���,����ЙC��ȥ���ʲ���,�ߜ��·�����K�a�﷽��ƫ�ơ�
 |
 |
�ɈD6��7�ɵñ��^���Ea���l������A(Ҋ��4)���Y������,����CODCr�ı��^��ܞ�:�ЙC�������ɽK�a���33.74kJ/mol,�����ɵͼ����6.58kJ/mol,�ɵͼ��������ɽK�a���31.60kJ/mol,��Ҋ�ЙC�������ɵͼ���ķ������^���M��,��ֱ��������ͼ��������ɽK�a����ٶȺ���,���ߜض���Ҫ�ӿ��˺�ɷN;���ķ����ٶȡ�
����
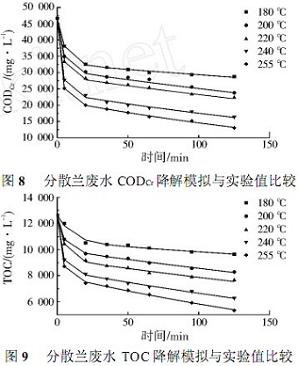
�ɱ�4�����W�����A�yCODCr��TOC������r(Ҋ�D8��9,�D�з�̖�錍��,����ģ���A�y),CODCr��TOC�A�yֵ�c���ֵ�ஔ�Ǻ�,CODCr��TOCȥ�������ƫ��քe��2.00%��1.80%,�f��ԓģ�ͽ�ጷ�ɢ�m�Uˮ�ĝ�ʽ�������^�^���Ǻ����ġ�
 |
3���Y��Փ
����
(1)�ض��ǏUˮ��ʽ�������P�IӰ�����,�������@���������Ч����
����
(2)�MˮCODCr46710mg/L��255�淴��2h,CODCrȥ�����_72.1%,�Uˮ�Ŀ������ԏ�0.15������0.69,ɫ����ȫ��ȥ��(ɫ�ȏ�5�f������50������),�f����ʽ������ԓ�Uˮ�����^��
��̎��Ч��,����Ч���A̎�����g��
����
(3)��ʽ����ǰ�ڳʬF���ɻ���������,������������ͨ�Ä����Wģ��,ԓģ���A�yֵ�c���ֵ���^���Ǻ�,����CODCr�ı��^���:�ЙC�������ɽK�a���33.74kJ/mol,�����ɵͼ����6.58kJ/mol,�ɵͼ��������ɽK�a���31.60kJ/mol��
�����īI
1��MishraVS,MahajaniVV.Wetairoxidation.Ind.Eng.Chem.Res.,1995,34(1):42��48
2��TeletzkeGH.Wetairoxidation.Chem.Eng.Pro.,1964,60(1):33��38
3��DietrichMJ.Wetairoxidationofhazardousorganicsinwaste water.Environ.Prog.,1985,4(3):171��177
4�����Ă�,�w����,��S,��.�Uˮ̎���Н�ʽ�������g�о��Mչ.�Ϻ��h���ƌW,1999,18(5):220
5TangWW,ZengXP,ZhaoJF,etal.The study on the wetair oxidation of highly concentrate demulsifed waste rwater and it ski2 netics.Separation and Purification Technology, 2003,31(4):77��82
6��LiL.Generalizedkineticmodelforwetoxidationoforganiccom2pounds.J.AICHE.,1991,37(11):1687��1697

ʹ����“��һ��”��������“���v�h���W”









