MAP���c��ʯ�����M�Ϲ�ˇ��Ó��������о�
ժҪ:�Ըߝ�ȵ���ģ�M�Uˮ��̎�팦��ͨ�^�o�B����о���MAP���������@�V�����c��ʯ�����M�Ϲ�ˇ��Ó������Ч������MAP������Ó����ij�ˮ�����ʯ�����^�̵��Mˮ����K��ˮ�ĵ�����ȥ���ʿ��_86.69%��99.9%������MAP�����^���в�ȡ�^�ߵ�pHֵ��Mg2+��������ں��ڷ�ʯ������������ȥ����
�P�I�~:MAP��,��Ȼ��ʯ,����,ȥ������Ӱ�����
1 ����
�S�����r�I���aҎģѸ�ٔU���˿ڲ������L���˂����a�����ŷų����д���������������ˮ���I�Uˮ��ʹˮ�РI�B���|�������������������������Ѹ�ٷ�ֳ��ˮ�w�ܽ������½����~������������������ˮ�|������Ҫ�ĸ����ϱ��Cˮ�|�����ȡһ����ˮԴ���o��ˮ̎����ʩ��
Ŀǰ�����Uˮ��̎�������кܶ࣬�����в�ͬ��ȱ�c�����䌦�ں��ߝ�Ȱ����������}�ďUˮ��һ�����������̎��Ч���������룬����Ҏ�Ļ��W�����������֕��a�������y��̎�������ࡣ20���o60����ԁ����˂��_ʼ�о����������@�V��Mgnesium Ammonium Phosphate��MAP��������ȥ���ͻ��ՏUˮ�еĵ���[1][2]���������ɵ������@�V��MgNH4PO4·6H2O[3]������һ�N�ܺõľ�ጻ��ʣ������ь��������Ј������˷����в���֮̎��Ԭ�i��[2]�Č��Y������������ȥ���ʸ��_90%���ϕr��������ȥ���ʃH��13%���_��������ͬ�r��Чȥ����Ŀ�ġ�
��ʯ��һ�N�ʹǼܠ�Y���Ķ���ԡ���ˮ���X���}���w���܉������ͽ����ض��Π�ʹ�С�ķ���[4]���������������кܺõ�Ч��������y�Ͳ�������Ȼб�l��ʯ̎���������Uˮ������ƽ��ȥ���ʞ�85%�����Ƶ�[6]�������m��[7]Ҳ���@���������о���
�ڱ���ԇ��У��M����MAP���c��ʯ������Y�ϵĽM�Ϲ�ˇ���_��ͬ�rȥ������Ч��������MAP���c��ʯ�������������^���У�MAP����Ҫ��pHֵ��9.5�� 11.0[2]�ĉA�ԗl�����M�У�����ҪͶ���^�����V�}���ܱ��C�ĸ�Чȥ��������Һ���^�ߵ�pHֵ�͚�����Mg2+�،������ڵķ�ʯ�����������Ӱ푡����Č��о����NӰ����،�ԓ�M�Ϲ�ˇ��Ӱ푣�������pHֵ����ʯ���������������������r�g���V�}���������ء�ּ���о�ԓ�M�Ϲ�ˇ�Ŀ������Լ�������ȥ��Ҏ�ɣ���MAP���ͷ�ʯ�����M�Ϲ�ˇ����ʽ�ṩ��Փ�����ͼ��g֧�֡�
2 ����
2.1 ģ�M�Uˮ������
�Qȡ0.2636g�������⛣�KH2PO4����2.0713g�Ȼ��@��NH4Cl������1Lȥ�x��ˮ������ģ�M�Uˮ��ԓģ�M�Uˮ�����|����ȣ���PӋ����60.0mg/L���������|����ȣ���NӋ����542.0mg/L��ģ�M����ij��ˮ�S����Óˮ����Һ�������c��Ħ���Ȟ�20��1�����������ˎ�������������
2.2 ����^��
2.2.1 ��Ȼб�l��ʯ��������
�Ҝؗl���������B���������M�зֽM����ԇ�D�ٶ���150r/min����ԇ�ȫ�^��ʹ�õľ����㽭�N�Ƶ���Ȼб�l��ʯ��
����1Lģ�M��ˮ����6��150ml��С�����зքe����100mL��ģ�M�Uˮ����һ�Mԇ�x��180��200Ŀ�����ķ�ʯ����ÿ��С�����м���6g���քe����20�� 120min����ÿ����Ʒ�o��2h���V���y����ˮ�еĵ��ם�ȣ��ó���ѷ����r�g���ڶ��Mԇ�x��120�� 200Ŀ������0.076��0.125mm���ķ�ʯ���քe��һ�����ķ�ʯ���뵽5��ʢ��ģ�M�Uˮ��С�����У�����һ���r�g��ԓ�r�g����ѷ����r�g�_�������y��ˮ�еĵ��ם�ȣ��ó���ѷ��������������M���x����������ķ�ʯ���քe������м���6��16g���y��ˮ�еĵ��ם�ȣ��ó����Ͷ������
2.2.2 MAP���c��ʯ�����M�Ϲ�ˇȥ������
����1 L ģ�M�Uˮ�� ����M g �� P �� Ħ���ȣ� =1.5��1��pH=10.0����ѷ����l��[8]����ʢ��ģ�M�Uˮ�ğ����м���0.3272g�����V��MgSO4������NaOH��Һ��pHֵ�{��10.0����150r/min�D������20min���ڴ����g�����CpHֵ�㶨��10.0�������Y�����o������V���y��ˮ�ĵ��ם�ȡ���MAP���ij�ˮ�����ʯ���������Mˮ������ѷ����r�g�������������������ėl���·������y����K��ˮ�ĵ��ם�ȣ�����ԓ�M�Ϲ�ˇ�Ŀ����ԡ��S��׃MAP�������ˮ��pHֵ�� MAP�������V�}��Ͷ�������о��䌦���ڷ�ʯ������Ӱ푣��y����K��ˮ�ĵ��ם�ȣ��ó�ԓ�M�Ϲ�ˇ������ȥ��Ҏ�ɡ�
2.3 ��������
ˮ��̎��������У��y���ם��ǰ��ȡˮ��Ѹ���� 0.45μm�ĞVĤ�^�V��
ˮ�ӷ����������Ї��h���ƌW���������ĵ��İ桶ˮ�͏Uˮ�O�y����������[9]�M�С������Ĝy�������c��ԇ���ֹ��ȷ����������}�Ĝy�������f�R���ֹ��ȷ���
3 �Y���cӑՓ
3.1 ��ʯ����ȥ�����Č��Y��
3.1.1 �����r�g������ȥ��Ч����Ӱ�
��ͬ�Ľ��|�r�gֱ��Ӱ���Ȼ��ʯ������ȥ��Ч�ʡ��ĈD1���Կ�������ʯ��������һ�����^Ѹ�ٵ��^�̣������������20min�ȣ�������ȥ�����_����61.77%���ֵİ������Ա���ʯ���������Q�� 80min�r��������ȥ���ʞ�70.65%���˺��S���r�g�����L��ȥ���ʻ�������׃������ʯ���������������S�r�g׃�������������20min�ȣ���ȥ�����_��16.18%��֮���S�������r�g�����L�������ϲ���׃����
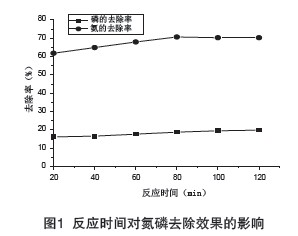 |
������ȥ������������r���^Ѹ�٣�B o o k e r���˵��o�B���Y��ָ���������������Q�����ڷ����_ʼ��10min�����[10]��Dimova���˵��о���������ƵĽY������ʯȥ��������һ���dz�Ѹ�ٵ��^�̣����� 15min[11]���@�N����ȥ���S���|�r�g��׃��Ҏ�ɻ������������������ʯ�Y�������е��������Qλ�ǿյģ���Һ�İ�������ݶȸߣ������������Q���ٶȷdz��죻����������������Qλ��u��ռ������Һ�а�����Ⱦ������ͣ�ȥ����څ�ڲ�׃[7]������ʯ�������������h�����������������������ڌ��H�����У�������߹���Ч�ʣ����ܟo���Ƶ����L�����r�g�������D1���Դ_����ѷ����r�g��80min��
3.1.2 ��ʯ����������ȥ��Ч����Ӱ�
��ʯ����������ȥ��Ч����Ӱ�Ҋ�D2��һ����f����ʯ����Խ�ࡢ����ԽС����������������Խ����Ч����Խ�á�ͨ�^�ڶ��M�����Կ�������ȥ�����S����ʯ�����ĜpС�����ߣ�����ʯ����С��һ���̶ȕr��ȥ������������
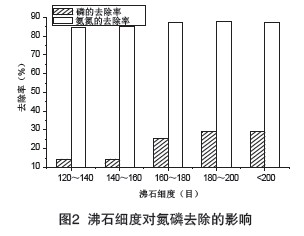 |
��ʯ������ԽС���ȱ���eԽ��λ������ʯ�Ŀɽ��Q�����c��Խ�࣬�������ȥ����Ҳ��Խ�ߡ����ڌ��H���a�У�����̫С�����ڲ���������Ѽ��ȴ_���� 180��200Ŀ��
3.1.3 ��ʯ����������ȥ��Ч�ʵ�Ӱ�
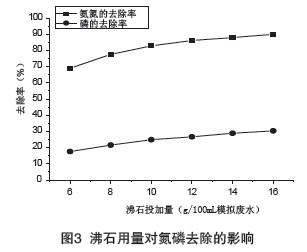
��ͬ������ֱ��Ӱ푷�ʯ��������������ʯ������ȥ��Ч���SͶ������׃��������D3��ʾ���ɈD3���Կ���������ȥ�����S��Ͷ���������Ӷ�Ѹ������������ʯͶ����Խ��������������Խ��ȥ����Ҳ��Խ�ߡ���Ͷ��������12g/100mLģ�M�Uˮ�r������ȥ���������������@�����̌��H�У����]���ɱ���Ͷ�������ܟo�����ӣ�����������_����12g/100mLģ�M�Uˮ��
 |
3.2 MAP���c��ʯ�����M�Ϲ�ˇȥ������
3.2.1 �M�Ϲ�ˇ��̎��Ч��
ģ�M�Uˮ�ij�ʼ���ם�ȷքe��5 4 2 . 0mg / L�� 60.0mg/L��������ѷ����l���M��MAP�����y�ó�ˮ�еĵ��ם�ȡ��ٌ��˷����ij�ˮ�����ʯ�����������Mˮ���y��K��ˮ�ĵ��ם�ȣ��������1��ʾ��
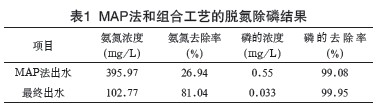 |
�ɱ�1���Կ�����M A P�����������ܸߵ�ȥ��Ч�ʣ������д����İ������ڡ����^��ʯ�������������r�g8 0mi n����ʯ����1 8 0��2 0 0Ŀ������ 12g/100mLģ�M�Uˮ���y�ó�ˮ�еİ����ĝ�ȴ���Ƚ��ͣ�MAP���c��ʯ�����M�Ϲ�ˇ��ȥ������Ч�����^�������܉��_��ͬ�rȥ���ɷN�I�BԪ�ص�Ŀ�ġ�
3.2.2 pHֵ���M�Ϲ�ˇȥ������Ӱ�
pHֵ�����ڷ�ʯ������������Ӱ푵ġ�ȡ���^ MAP���������ˮ�ӣ���pHֵ�քe�{��6.0��8.0�� 10.0��Ͷ��һ�����ķ�ʯ��12g/100mLģ�M�Uˮ���M�������������y����K��ˮ�ĵ��������2��ʾ��
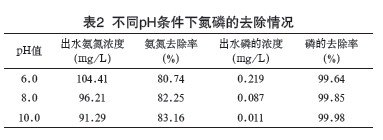 |
�ɱ�2�������Կ�����pHֵ������Ӱ푲����������Ҫ��ǰ�ڵ�MAP�����ѽ�����ȥ������pHֵ��������ȥ��߀����һ��Ӱ푵ģ�������ȥ�����S��pHֵ�������������ӡ��@��Ҫ�����ڏUˮ��NH4+�cNH3���������µĻ��Wƽ���Pϵ:
����Һ��pH�^�͕r���Uˮ�е�H+�x�ӝ�����ӣ�������Ҫ��NH4+��ʽ���ڣ��������������õİl��������Һ��H+����^�ߕr��H+��ֱ����0.24nm����NH4+�� 0.286nm����H+��NH4+�����M���ʯ���ȣ��c��ʯ�ϵĽ�����x�Ӱl�����Q������NH4+���ܱ���ʯ����������Q��ʹ�ð���ȥ��Ч���
����Һ��pHֵ���ߕr��������Ҫ��NH3·H2O���ڣ�NH4+�p�٣��mȻ��ʯ�������Üp�������ݳ��İ���ռ������ʣ��İ�����Ƚ��ͣ���ȥ���ʳ��m���ߡ����@������ɴ��Ķ�����Ⱦ���҉A��Ͷ�ӕ����̎���ɱ����ӣ�����Һ��pHҲ�����^�ߡ�
3.2.3 Mg2+�������M�Ϲ�ˇȥ������Ӱ�
ͨ�^�{��MAP�����V��Ħ���ȁ���׃ˮ��Mg2+�ĺ�����̽ӑMg2+���������ڷ�ʯ������Ӱ푡����Mƽ�Ќ���зքe���V�ױ��O��1��1��1.5��1��2��1���ó��Č��Y�����3��ʾ��
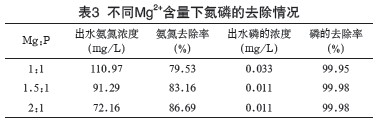 |
�ɱ�3���Կ�����Mg2+����Խ�ߣ���ȥ�����������ӣ�����������ȥ���������@��Ӱ푡����^MAP������Һ��Mg2+ʣ����Խ�࣬��ʯ������������ȥ��Ч��Խ�á�Ԭ�i[2]��ͨ�^���ó�ˮ��Һ�е�Mg2+��ȵ���ߕ����MMAP�Y���������M�С�
�@�����������@�V�γɵķ���ʽ���£�
��ˮ��Һ��Mg2+�����^�ߕr�������ڷ������M�У�ʹMAP���ij�ˮ�е��ם�Ƚ��ͣ��p�p���m��ʯ����������ؓ�ɣ���K�õ�����99.98%��������86.69%������Ч����
4 �YՓ
��1���Ϊ����÷�ʯ���x�ӽ��Q�c����ȥ����ˮ�е��וr����ѕr�g��80min����ѷ�ʯ���Ȟ�180��200Ŀ��������0.076��0.088mm����������12g/100mLģ�M�Uˮ����������ȥ���ʿ��_85.17%������ȥ���ʃH��26.75%��
��2���ڽM�Ϲ�ˇ�l���£�����ѷ����l������ MAP���ij���Ч�������Է�ʯ��������ߌ�������ȥ���ʣ����_��ͬ�r��Чȥ������Ŀ�ġ�
��3�����MAP��������Һ��pHֵ��Mg2+�ĝ�ȣ����ܴ��MMAP�Y�����������CMAP���ij���Ч�����������ں��ڷ�ʯ�����������������M�У���ʹ������ȥ���ʷքe�_��80%��99%���ϡ�
�����īI��
[1] �������_��Դ.���ᰱ�V���g�đ����о�[J].ˮ̎�����g��2007��33��3���� 1-5.
[2] Ԭ�i����������Ԭ������.���ᰱ�V�Y����ȥ���ͻ����B�i�Uˮ�РI�BԪ�صČ���о�[J].�h���ƌW�W��2007��27��7����1127-1134.
[3] ��������ϯ����������������.���ᰱ�V����ȥ���c���ՏUˮ�е��đ����о��Mչ[J].�����Mչ��2007��26��3����371-376.
[4] �ؖ|�x.��Ȼ��ʯ����-�����������g�����ڵ�������ꏽ����Ⱦ�����е�ԇ��c�C���о�[M].�������Ї��h���ƌW������.2003.
[5] ����y������.��Ȼ��ʯ̎�������Uˮ���r������о�[J].���ջ�����2001��27 (2����32-35.
[6] ���ƣ�ꐅ�܊���ؖ|�x.��Ȼ��ʯ����Һ�а����������Ե��о�[J].���B�h��. 2006��15��2����219��223.
[7] �����m����ʥ����ꐳ�ѩ��.��Ȼ��ʯ�����}�V����Ó������Ч��[J].ˮ̎�����g.2007��33��11����71��74.
[8] �����ƣ��ܘs�����ܷ�����.���ᰴ�V������������ˮ���ķ����l������ [J].���I��ˮ�c�Uˮ,2008,39(1)��58-61.
[9] ˮ�͏Uˮ�O�y�������������İ棩[M].����:�Ї��h���ƌW������.2002.
[10] N.A.Booker,E.L.Cooney��A.J.Priestley.Ammonia removal from sewage using natural Australian zeolite.Water.Sci.Technol.1996�� 34:17-24.
[11] G Dimova,G Mihailov��Tz.Tzankov.Combined filter for ammonia removal-Part��Minimal zeolite contact time and requirements for desorption.Water.Sci.Techno.1999��39��123-129.

ʹ����“��һ��”��������“���v�h���W”









